伊莱博生物科技(上海)有限公司
17 年
手机商铺
- NaN
- 0.7999999999999998
- 0.7999999999999998
- 2.8
- 2.8
技术资料/正文
《Hepatology》解读:STK24-MASTL-YBX1-PAK4轴——肝细胞癌仑伐替尼耐药的新机制
13 人阅读发布时间:2026-05-09 15:23
《Hepatology》解读:STK24-MASTL-YBX1-PAK4轴——肝细胞癌仑伐替尼耐药的新机制

Ø 研究背景
肝细胞癌(HCC)是全球最常见且致死率最高的恶性肿瘤之一,主要由慢性肝病和肝硬化引起。尽管系统治疗取得了进展,但晚期HCC的预后仍然很差。仑伐替尼(Lenvatinib)作为一种多激酶抑制剂,通过靶向VEGFR、FGFR、PDGFR和RET等多种激酶发挥抗肿瘤作用,已成为HCC的一线治疗药物。然而,仑伐替尼的疗效常因肿瘤产生耐药性而受限,仅能延长患者数月的生存期。因此,阐明仑伐替尼耐药的分子机制对于改善临床结局和发现潜在治疗靶点至关重要。
微管相关丝氨酸/苏氨酸激酶样蛋白(MASTL)是一种AGC家族激酶,最初在果蝇中被发现,通过抑制蛋白磷酸酶2A复合物(PP2A)调控细胞周期进程和有丝分裂。近年研究表明,MASTL在多种癌症中促进肿瘤进展和治疗耐药,如乳腺癌的放射耐药、结肠癌的化疗耐药以及口腔鳞状细胞癌的顺铂耐药。然而,MASTL作为激酶在耐药相关信号通路中的作用研究较少。本研究旨在探索MASTL在HCC仑伐替尼耐药中的具体机制,并寻找克服耐药的新策略。
Ø 研究结果
2.1 整合转录组学和蛋白质组学分析揭示MASTL在仑伐替尼耐药的HCC细胞和组织中高表达
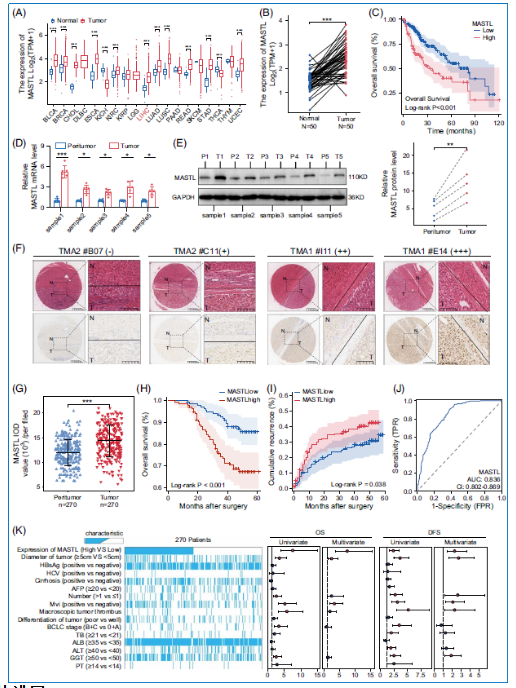
研究者建立了两株仑伐替尼耐药细胞系(PLC/PRF/5-R和MHCC97H-R),通过IC50测定、克隆形成实验和细胞活力检测确认其耐药性。同时,获取了6例仑伐替尼耐药或敏感患者的活检样本。转录组测序和蛋白质组测序分析显示,在耐药细胞和组织中有7个共同上调基因,其中MASTL因其与多种治疗耐药相关而被选为研究对象。进一步验证表明,MASTL在耐药细胞和组织中表达显著升高。研究者还构建了独特的药物治疗组织芯片,包含52例仑伐替尼治疗患者的手术样本,免疫组化结果显示MASTL高表达的患者中疾病稳定(SD)比例更高,且分层生存分析显示MASTL高表达的仑伐替尼治疗患者预后更差。这些结果突出了MASTL在仑伐替尼耐药中的潜在重要性。
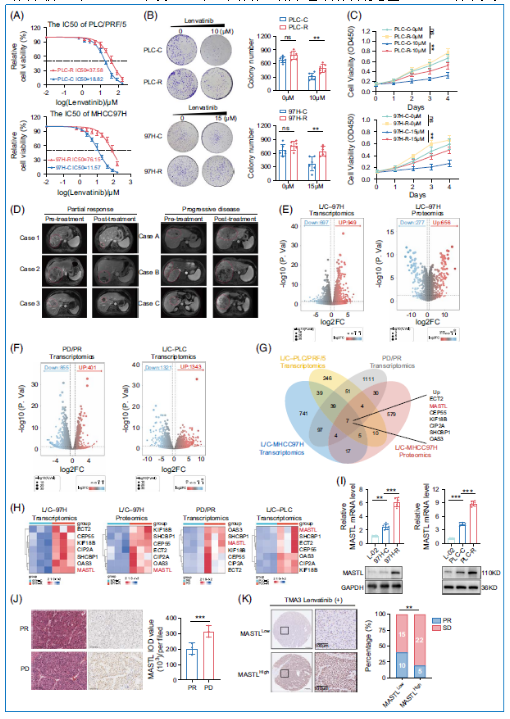
2.2 MASTL过表达与HCC患者不良预后相关
利用TCGA数据库分析,研究者发现包括HCC在内的多种癌症中MASTL在肿瘤组织中的表达高于正常组织。HCC患者中MASTL高表达与更短的总生存期(OS)相关。这一发现通过5对HCC样本及配对正常组织的qRT-PCR和免疫印迹实验得到验证。在TMA1和TMA2队列中,MASTL高表达与恶性表型和不良预后相关,AUC值为0.836,表明其具有较高的诊断准确性。多变量Cox回归分析显示,MASTL高表达是OS和无病生存期(DFS)的独立预测因子。因此,MASTL成为与HCC不良预后相关的关键基因。
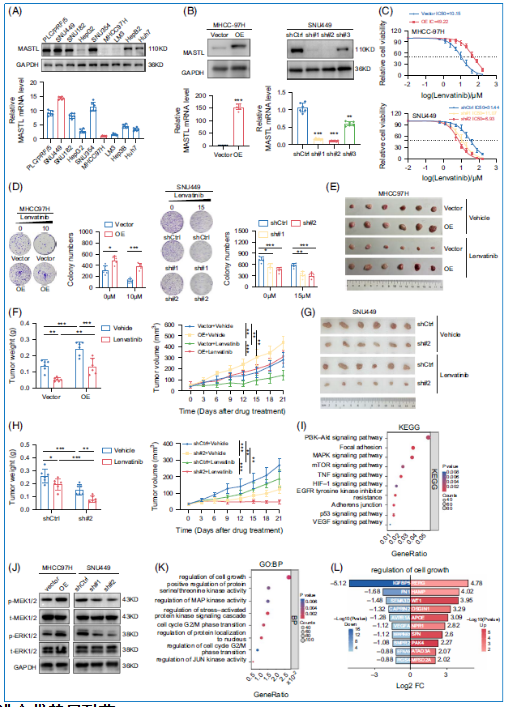
2.3 MASTL促进HCC细胞仑伐替尼耐药和体内外进展
MASTL在不同HCC细胞系中的表达水平与仑伐替尼IC50值呈强正相关。通过构建MASTL过表达和敲低的慢病毒载体,研究者发现MASTL过表达降低细胞对仑伐替尼的敏感性,而MASTL敲低则增强敏感性。MASTL过表达还促进细胞迁移、侵袭和自我更新能力。体内成瘤实验表明,MASTL敲低显著抑制肿瘤生长和仑伐替尼耐药,而MASTL过表达则增强肿瘤生长和耐药。RNA测序的KEGG分析显示MASTL高表达激活MAPK信号通路,GO分析显示其与细胞生长调控相关。这些发现表明MASTL通过调控MAPK信号通路显著促进肿瘤生长并赋予仑伐替尼耐药。
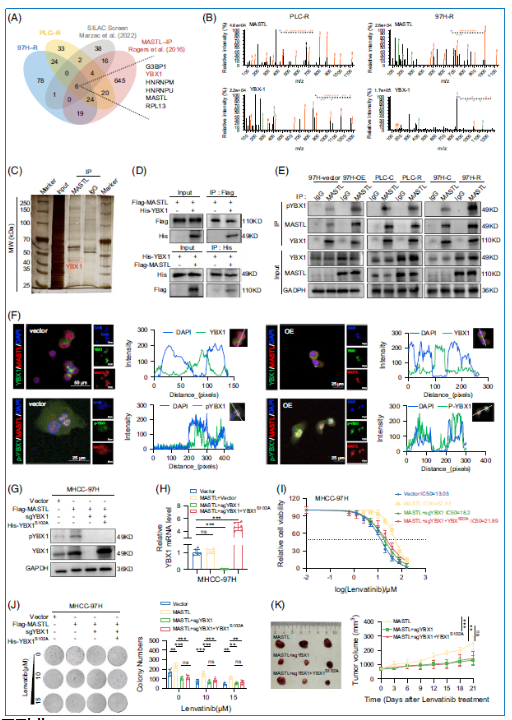
2.4 MASTL通过促进YBX1的磷酸化和核转位促进仑伐替尼耐药
通过免疫共沉淀和质谱分析,研究者在耐药细胞中鉴定了MASTL的相互作用蛋白,并与已发表的MASTL相互作用数据集交叉比对,最终确定Y-box结合蛋白1(YBX1)为关键底物。LC-MS/MS数据、银染和免疫印迹验证了MASTL与YBX1的结合。通过构建截短质粒,发现YBX1的Ala/Pro富集N端(AP)结构域和冷休克结构域(CSD)负责与MASTL相互作用。鉴于YBX1在S102位点的磷酸化(p-YBX1)是其活性形式,研究者发现MASTL表达变化直接影响p-YBX1水平和YBX1稳定性。耐药细胞中YBX1磷酸化显著增加,免疫荧光显示MASTL与p-YBX1在MASTL过表达细胞的细胞核中强烈共定位。核质分离实验进一步证实MASTL过表达与YBX1在细胞核中的过度磷酸化相关。通过敲除YBX1并转染S102突变体(YBX1-S102A),发现MASTL诱导的仑伐替尼耐药在YBX1敲除后降低,且不能被突变YBX1的重新表达所逆转,表明YBX1的磷酸化对MASTL介导的耐药至关重要。
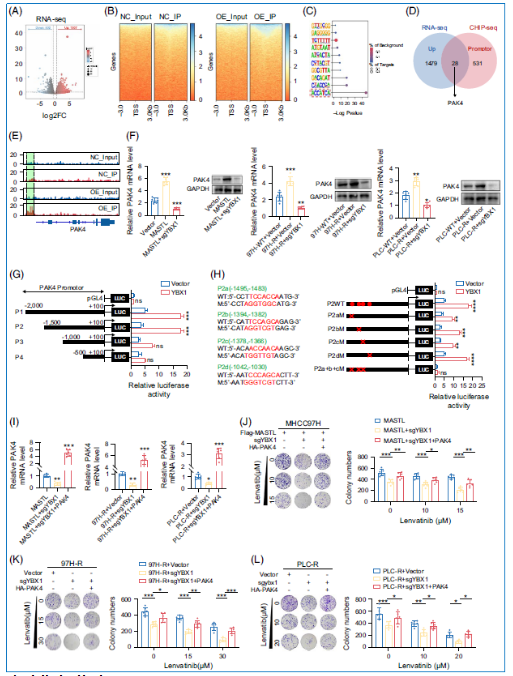
2.5 磷酸化YBX1通过转录激活PAK4促进仑伐替尼耐药
为鉴定YBX1的靶基因,研究者进行了RNA测序和染色质免疫共沉淀(ChIP)实验。结果显示MASTL高表达激活YBX1的转录功能,在基因组转录起始位点附近鉴定出更多YBX1结合区域。通过RNA-seq与ChIP-seq数据交叉,获得28个重叠基因,其中p21激活激酶4(PAK4)因其在调控细胞存活和耐药中的作用被选为研究对象。ChIP-seq结果显示YBX1在PAK4启动子区域显著富集。荧光素酶报告基因实验表明PAK4启动子的-1500至-1000区域足以介导YBX1的转录激活,该区域内4个推定的YBX1结合位点中,a、b、c位点的突变部分降低YBX1介导的PAK4启动子活性,而联合突变完全消除该活性。在YBX1敲除的MASTL过表达细胞中恢复PAK4表达,部分挽救了仑伐替尼耐药的降低,并帮助MASTL重新激活MAPK信号通路。这些结果表明PAK4是MASTL介导仑伐替尼耐药的关键效应分子。
2.6 应激激活的STK24导致MASTL在S875位点的磷酸化和激活
MASTL在T194、T299和S875位点存在保守的磷酸化位点。通过丙氨酸突变实验,发现S875突变显著损害MASTL磷酸化YBX1的能力,表明S875对MASTL的激酶活性至关重要。S875突变还降低细胞对仑伐替尼的耐药性,并阻止MASTL的核转位。将LC-MS/MS免疫共沉淀数据与常见人类丝氨酸/苏氨酸激酶列表交叉比对,鉴定出丝氨酸/苏氨酸蛋白激酶24(STK24,也称MST3)是唯一候选激酶。免疫荧光和免疫共沉淀显示MASTL与STK24存在结合相互作用。STK24在氧化应激和缺氧条件下被磷酸化激活,而仑伐替尼处理以剂量和时间依赖的方式激活STK24磷酸化。由于缺乏MASTL S875位点的磷酸化特异性抗体,研究者通过监测MASTL的核定位间接评估其磷酸化程度。STK24敲低显著降低MASTL核转位的效率,表明STK24确实影响MASTL S875的磷酸化。这些发现突出了S875对MASTL功能的关键重要性,并提示仑伐替尼可能通过STK24调控MASTL磷酸化。
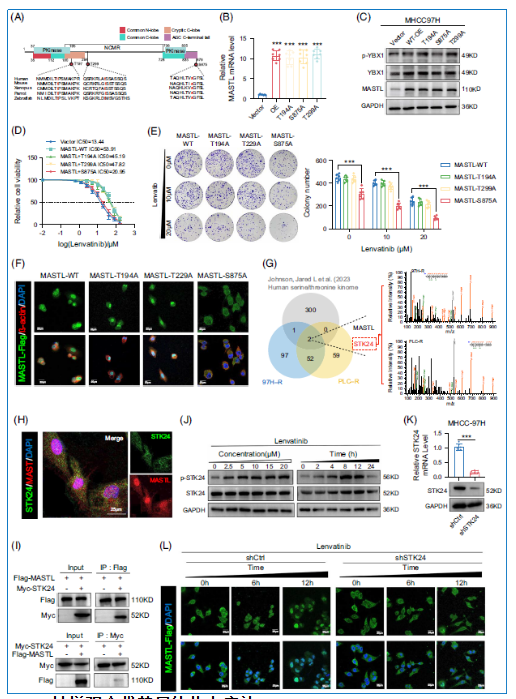
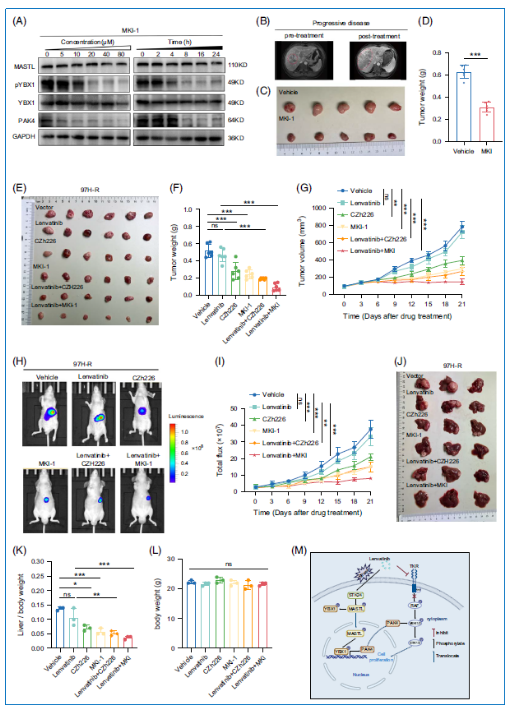
2.7 靶向MASTL的MKI-1通过抑制MASTL/YBX1/PAK4轴增强仑伐替尼的体内疗效
临床样本证实,野生型YBX1和磷酸化YBX1在HCC组织中显著高于配对正常组织,且其表达与HCC预后负相关。TMA1队列中MASTL、YBX1、p-YBX1和PAK4高表达频繁共存,且疾病进展(PD)患者相比部分缓解(PR)患者呈现过度激活的MASTL/YBX1/PAK4轴。鉴于该轴在仑伐替尼耐药中的关键作用和MASTL的核心调控地位,研究者选择MASTL抑制剂MKI-1阻断该轴。免疫印迹显示MKI-1以剂量和时间依赖的方式抑制MASTL/YBX1/PAK4轴的激活。使用仑伐替尼耐药患者的肿瘤标本构建PDX模型,MKI-1处理显著抑制耐药肿瘤生长。在皮下和原位移植瘤模型中,虽然单用仑伐替尼效果有限,但MKI-1或PAK4抑制剂CZh226联合仑伐替尼显著抑制肿瘤生长,且MKI-1联合仑伐替尼的疗效优于其他治疗组合。此外,联合治疗未引起体重变化或明显副作用。在5例MASTL高表达患者来源的PDX模型中,联合治疗同样显著抑制肿瘤生长。
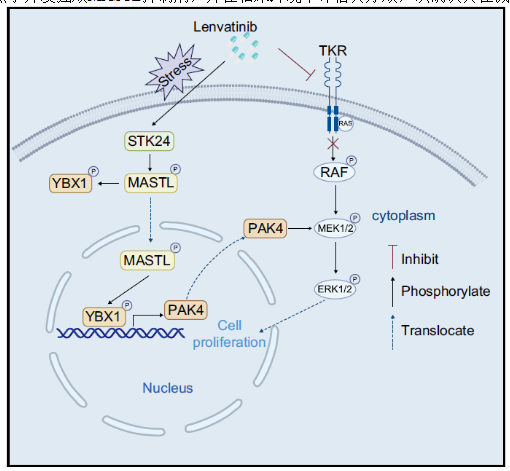
Ø 研究结论
本研究揭示了MASTL/YBX1/PAK4信号轴是驱动HCC仑伐替尼耐药和肿瘤进展的关键机制。仑伐替尼暴露下,应激激活的STK24磷酸化MASTL的S875位点,激活MASTL的激酶功能;活化的MASTL进而磷酸化YBX1的S102位点,促进其核转位并激活转录因子功能;磷酸化YBX1转录激活PAK4,通过MAPK信号通路促进细胞存活和增殖,最终导致仑伐替尼耐药。靶向抑制该轴(特别是使用MASTL抑制剂MKI-1)可在体内外模型中显著增强仑伐替尼的疗效,为克服HCC仑伐替尼耐药和改善患者临床结局提供了潜在的新型治疗策略。未来研究应聚焦于开发强效MASTL抑制剂,并在临床环境中评估其疗效,以确认其在减轻仑伐替尼耐药方面的潜力。
Ø 研究思路
该研究遵循"现象发现→机制探索→功能验证→转化应用"的经典研究范式:
1.临床问题出发:针对HCC仑伐替尼耐药的临床难题,建立耐药细胞系和获取患者样本;
2.组学筛选靶点:通过转录组学和蛋白质组学整合分析,筛选出关键耐药基因MASTL;
3.临床相关性验证:利用TCGA数据库、临床样本和组织芯片,验证MASTL与HCC预后和仑伐替尼疗效的关系;
4.功能机制研究:通过体内外实验明确MASTL促进耐药和肿瘤进展的功能,并深入解析其下游分子机制——MASTL→YBX1磷酸化/核转位→PAK4转录激活→MAPK通路激活;
5.上游调控机制:发现STK24作为应激响应激酶,在仑伐替尼刺激下激活并磷酸化MASTL的S875位点,启动整个信号轴;
6.转化应用验证:使用MASTL抑制剂MKI-1和PAK4抑制剂CZh226,在多种体内模型(皮下瘤、原位瘤、PDX模型)中验证联合用药克服耐药的效果,为临床应用提供实验依据。